Diez campesinos del municipio Guanarito, al sureste del estado Portuguesa, habían muerto de un virus desconocido. Al principio se pensó que era dengue porque había un brote y porque producía fiebres altas y dolores musculares. Pero luego, aparecían fuertes dolores de cabeza, vómitos, convulsiones y hemorragias violentas. Parecía ébola. Mataba a los enfermos en menos de una semana. No había nada similar en Venezuela. Era algo nuevo. Los campesinos no sabían cómo se transmitía. Nadie podía protegerse.
Era el año 1989. El Laboratorio de Virus Animales del Instituto Venezolano de Investigaciones Científicas (IVIC) y el Instituto Nacional de Higiene (INH) monitoreaban la aparición de patógenos para prevenir epidemias. Eran parte del sistema de vigilancia epidemiológica en Venezuela. De las muestras de dengue que llegaron al INH, varias dieron negativo. El laboratorio del IVIC envió a Juan Carlos Navarro, un biólogo recién egresado de la Universidad Central de Venezuela, a recoger muestras. Debía descubrir qué estaba matando a la gente.
Juan Carlos y Humberto Montañez, un técnico del laboratorio, llegaron a la zona del brote en una camioneta vieja de la Escuela de Malariología del Ministerio de Sanidad. Identificaron a los enfermos e interrogaron a la comunidad para entender mejor los síntomas y la progresión del posible virus. Luego preguntaron por sus rutinas, sitios de trabajo, alimentación, fuentes de agua, viajes y cualquier otra información que revelara posibles nexos entre los casos. Los puntos en común podrían apuntar hacia el origen del virus, pero más allá de vivir en la misma zona, no había nexos.
Los campesinos estaban asustados. Las hemorragias desangraban a la gente. Un hombre se enfermó en el campo, regresó a casa y contagió a su esposa, le contaron. Ambos murieron. Juan Carlos se preocupó. Quizás el virus se transmitía entre humanos, pero ¿cómo? ¿Saliva, secreciones, transmisión sexual? ¿Y de dónde venía? ¿Cómo había aparecido?
Guanarito está en los llanos. Hace dos siglos la región estaba cubierta por bosques tropicales, pero los humanos deforestaron, transformaron los bosques en sabanas para construir viviendas y sembrar. Ahora las poblaciones humanas, especialmente las que viven cerca de parches boscosos, como los agricultores, que aprovechan la fertilidad de esas tierras para sembrar, están en contacto frecuente con animales silvestres que viven allí.
Al ver el lugar, Juan Carlos pensó que el virus era de origen animal. El 70% de las enfermedades infecciosas emergentes y reemergentes, lo son. Los campesinos entraban y salían de los bosques, quizás habían cazado y comido un animal con el virus, o matado alguno durante la cosecha, contaminando el cultivo. Los mosquitos que picaban durante la faena también podían haber picado a monos, roedores, mamíferos pequeños o reptiles. Entre muchas posibilidades había un denominador común: el virus de Guanarito debía ser una zoonosis, una enfermedad animal que se traspasó a un humano.

Juan Carlos y Humberto entraron al bosque y atraparon mosquitos, garrapatas, roedores, aves, monos y extrajeron muestras. Hicieron lo mismo con animales que estaban cerca de las casas. No necesariamente son las mismas especies. Tenían que buscar muchas especies para aumentar la posibilidad de encontrar el “reservorio” del virus, la población animal donde circula el virus naturalmente. Los virus no sobreviven ni se reproducen solos, deben encontrar un organismo y usar la maquinaria de sus células para replicarse. Los “reservorios” son los animales u hospedadores naturales que mantienen el virus circulando en un sitio, tienen el virus presente en el cuerpo pero no se enferman.
Juan Carlos también buscó un posible vector, una especie que sirve de intermediaria, transmitiendo el virus del reservorio animal a un hospedador intermediario o a un hospedador final. Los insectos son los vectores más importantes y de ellos, los mosquitos son los que más enfermedades infecciosas transmiten. En Venezuela son vectores de la fiebre amarilla, malaria, zika, chikungunya, dengue, mayaro y otras enfermedades.
Las hemorragias de los campesinos hacían pensar a Juan Carlos que podía ser fiebre amarilla. Buscó lluvia de monos en el bosque. La fiebre amarilla puede ser mortal para algunos monos como los araguatos o monos aulladores y, cuando los afecta, caen de los árboles en grandes cantidades, como lloviendo sus cadáveres. Es evidencia de brotes de la enfermedad. Pero no vio monos muertos en Guanarito. Tenía que encontrar el animal responsable para descifrar cómo el virus había “saltado” a los humanos.
Juan Carlos dormía en la casa de un campesino, en una hamaca. Meciéndose, pensaba en el virus misterioso. No debía ser transmitido por mosquitos, porque entre que un mosquito pique al animal infectado y luego a un humano, y haga lo mismo para infectar a otras personas, debe pasar tiempo. Este virus se mueve más rápido. La mayoría de los enfermos eran hombres. En esa comunidad, los hombres pasan el día en el campo. Las mujeres en casa. Debía ser algo que tenía mayor presencia en el campo, pero que estaba en ambos lugares. Mientras buscaba puntos en común, vio una rata caminando sobre una viga en el techo. La rata atravesó la casa y se escondió dentro de los sacos de granos cosechados, almacenados en el garaje. Quizás eran las ratas.
Juan Carlos y Humberto pasaron dos semanas en Guanarito recogiendo muestras de pacientes y animales. Realizaron un informe con notas de campo, observaciones y sospechas. Llegando a Caracas, la camioneta de Malariología se accidentó. Humberto agarró la cava pequeña y cogió un autobús en la Panamericana. Junto a decenas de pasajeros, las muestras del virus mortal llegaron al Instituto Nacional de Higiene (INH). Dos semanas después, Juan Carlos recibió una llamada: debía hacerse exámenes urgentes.
Habían logrado aislar el genoma del virus y lo compararon con otros patógenos conocidos. Era un virus nuevo, similar a uno detectado en Argentina, pero con diferencias importantes. Lo llamaron “Guanarito”. Las enfermedades virales se nombraban a partir del lugar donde se detectaban primero: Ébola es un río en la República Democrática del Congo, Zika un bosque en Uganda. A partir de 2015, la Organización Mundial de la Salud recomendó un cambio en la práctica para evitar impactos negativos en la cultura y en la economía de estos lugares. Guanarito era el primer Arenavirus detectado en Venezuela, una familia de virus normalmente transmitidos por roedores a través de su orina, sangre, saliva o secreciones, que generan infecciones severas. En el Instituto Nacional de Higiene querían saber si Juan Carlos tenía síntomas o anticuerpos. El virus no tiene cura y mueren alrededor del 25% de los infectados.
Entre 1989 y 1995 hubo al menos 105 casos de Guanarito; 34% fueron mortales. Luego desaparecieron los casos humanos por seis años. En 2001 hubo otro brote y, a partir de 2005, hubo casos todos los años hasta 2016, el último año del que se tienen cifras oficiales. Durante los brotes, coinciden roedores infectados y humanos en el mismo lugar, pero todavía no se entienden todas las condiciones que los producen.
Guanarito es considerado un arma biológica categoría A, la más peligrosa, por el Centro de Control de Enfermedades (CDC) de Estados Unidos. Implica que el virus pone en riesgo la seguridad nacional y salud pública y debe ser manejado con extrema responsabilidad y medidas estrictas de bioseguridad. El virus se puede transmitir por partículas microscópicas en el aire, en forma de aerosol. Guanarito comparte la categoría junto al ántrax, la peste bubónica, el botulismo y el ébola, entre otros. Todas las anteriores son zoonosis.
Juan Carlos creció cerca de animales y sus enfermedades. De pequeño visitaba las fincas de tíos, en los llanos del estado Bolívar, viendo al veterinario vacunar al ganado y a los caballos. Siempre parecía haber una conexión entre mosquitos, pulgas, garrapatas y las enfermedades. Para su tesis de biología de la Universidad Central de Venezuela perdió el miedo a las alturas para guindar recipientes de bambú en árboles de 30 metros en Panaquire, estado Miranda, y recolectar mosquitos transmisores de fiebre amarilla a diferentes alturas y en diferentes periodos del año. Con los resultados entendió que estos insectos vivían en las copas de los árboles y bajaban cuando las copas perdían humedad por la incidencia solar. En sequía bajaban más que en periodos lluviosos. En esos momentos aumentaba el riesgo de contagio de fiebre amarilla. El comportamiento de los mosquitos influía en la transmisión de la enfermedad.
Como investigador en la UCV pasó tres años visitando 17 parques nacionales en Venezuela a fin de estudiar las especies de mosquitos que crecían en las cavidades de plantas que acumulan agua, como bromelias y heliconias. Quería entender mejor la distribución de algunas especies de mosquitos, entre otras cosas. En la cima del Auyantepuy, abría su carpa por la noche y encendía la linterna para atraer mosquitos. Cuando había suficientes, cerraba la puerta y los atrapaba uno por uno. Uno de ellos fue nuevo para la ciencia. Lo llamaron Anopheles auyantepuiensis. También encontró que la fauna que crece dentro de estas cavidades en plantas de Nueva Esparta es muy similar a la de Barlovento. Pero Nueva Esparta es una isla. Juan Carlos afirma que es evidencia de que hace miles de años, Nueva Esparta estaba conectada con tierra firme. Este proyecto sumó información sobre la distribución geográfica de especies de mosquitos vectores de enfermedades, ayudando a identificar áreas de riesgo.
El doctorado de Juan Carlos coincidió con un auge en la investigación de enfermedades zoonóticas en Venezuela. En vez de ser un sistema de vigilancia pasivo, que esperaba la aparición de un brote para estudiarlo y actuar, el sistema fue activo, los investigadores salían al campo a buscar las enfermedades antes de que brotaran. El INH, del Ministerio de Salud, trabajaba con el Instituto Nacional de Investigaciones Agropecuarias (INIA), el IVIC, el Laboratorio de Biología de Vectores de la UCV y las universidades. Además, universidades extranjeras como la Universidad de Texas en Galveston y la Universidad de Yale, así como algunos institutos gubernamentales extranjeros como el Instituto Nacional de Salud de Estados Unidos o el Ministerio de Salud de Colombia, financiaron investigaciones en Venezuela. El descubrimiento de Guanarito puso al país en el mapa epidemiológico regional. Lo mismo ocurrió con la Encefalitis Equina Venezolana (EEV), un virus identificado por primera vez en 1938.
En mayo de 1995, los caballos, las mulas y los burros en el sureste de Falcón, estaban aturdidos. Deambulaban como somnolientos, se alteraban, actuaban como locos, y luego caían muertos. En junio, poblaciones cercanas al río Tocuyo y Chichiriviche, desarrollaron fiebres, dolores musculares, vómitos y diarreas. Algunas personas se sacudían en el aire y se mordían los labios, convulsionando. Otras, entraban en un estado de confusión. Su cerebro se inflamaba. A veces morían.
El virus se movió a Yaracuy, luego a Lara, Zulia, Carabobo, Cojedes y Guárico. Luego entró a Colombia por la Península de La Guajira. En Riohacha, Colombia, llamaron al virus la “plaga de la locura” (mad plague), reportó The New York Times el 26 de octubre de 1995. Ese brote enfermó entre 75.000 y 100.000 personas y mató alrededor de 300 en Venezuela y Colombia. La EEV afectaba principalmente a equinos (caballos, burros y mulas), pero también enfermaba a los humanos, produciendo fiebre, malestar general, vómito, diarrea y, en casos graves, síntomas neurológicos, encefalitis y la muerte.
Entre 1938 y 1995, la EEV produjo brotes epidémicos en 12 países del continente, incluyendo una epidemia que comenzó en Guayaquil, Ecuador, subió por la costa atlántica de sudamérica, atravesó centroamérica y llegó a Texas, Estados Unidos, en 1971.
EEV también es considerada un arma biológica categoría B, por el CDC de Estados Unidos, menos mortal y transmisible que Guanarito. Aunque el EEV no suele ser mortal, es infeccioso, se necesitan pocas partículas de virus para producir una enfermedad, y los síntomas incapacitan a los enfermos. Durante la Guerra Fría, los Estados Unidos y la Unión Soviética trabajaron para convertir la EEV en arma biológica, según una investigación de Eric Croddy del Instituto de Estudios Internacionales de Monterey. En 1959, un contenedor de vidrio con partículas liofilizadas del virus se cayó y se quebró en la escalera de un laboratorio en la Unión Soviética. Las partículas microscópicas se diseminaron en el aire y 20 trabajadores enfermaron.
Juan Carlos, junto a Scott Weaver y su grupo, analizaron las muestras de EEV de los brotes de los setenta y noventa en Galveston, una isla al sureste de Houston, en el Centro Mundial de Referencia para Virus Emergentes y Arbovirus, de la Universidad de Texas. También examinaron mosquitos que recolectaron entre Brasil y los Everglades, en Florida. A Juan Carlos le llamaba la atención que la EEV no tenía ancestros en Asia, África o Europa. Muchos virus que hoy amenazan a la región americana vienen de otros lugares: la fiebre amarilla y el dengue se originaron en África. Pero los más afectados por EEV, los caballos, mulas y burros, no son americanos. Fueron traídos durante la colonia.

Un virus de origen americano afecta principalmente a animales no americanos. ¿Por qué? Las especies silvestres originarias del continente tenían miles de años viviendo con el virus. Algunos no eran susceptibles, pero los que se enfermaban y sobrevivían, desarrollaron inmunidad. Los que no, morían. Cuando entran especies nuevas, esta dinámica puede cambiar. Los equinos no evolucionaron con el virus y eran susceptibles. La colonización, hace unos 500 años, es reciente. Al introducir equinos en el continente, los humanos generaron una disrupción en el ciclo selvático del virus.
Juan Carlos cree que la EEV tenía miles de años circulando en roedores silvestres en el continente. Son el reservorio, no se enferman. Cuando entraron los equinos, un mosquito que también se alimentaba de la sangre de los roedores, picó a un caballo, mula o burro y encontró, accidentalmente, un hospedador intermediario más grande con más sangre, que pudo amplificar el virus rápidamente. También por accidente, un mosquito picó al equino, y luego picó a un humano, generando la primera infección en una persona. Pero las probabilidades de que esa cadena ocurriera son pequeñas.
Aún cuando el mosquito pica a esa cadena, no necesariamente transmite el virus. Cada virus tiene algunas especies de vectores posibles. No todos los mosquitos transmiten el virus. Además, con cada paso del virus por un organismo pueden ocurrir mutaciones en el virus, en el vector (en este caso, el mosquito), en el hospedador (caballo y humano) y en el reservorio (roedor), que pueden cambiar la ecuación.
En el laboratorio de Galveston, Juan Carlos trabajó con mosquitos de varios países que transmitían el virus y también con las partículas de virus. Hizo cócteles con muestras (sueros), agregó una enzima llamada polimerasa, y unos primers, que se anclan al material genético del virus. Los metió en un termociclador, o máquina de PCR, y programó varios ciclos. La máquina eleva y baja la temperatura para separar las hebras del ADN o ARN, las moléculas que contienen el material genético del virus, y amplificarlo. Con cada ciclo el número de moléculas se duplica. Después de 30 o 40 ciclos puedes obtener más de mil millones de copias de un gen. Juan Carlos se aseguró que las muestras tenían virus y las mandó a secuenciar, es decir, decodificar y amplificar el material genético. Le mandaron un archivo con una línea que tenía picos y valles. Parecía la silueta de una canción. En un programa de computación, comparó esa silueta con las de otros virus. La silueta genética es como una huella digital, es única para cada virus. El programa usa un algoritmo matemático para hacer comparaciones rápidas con millones de secuencias y te arroja similitudes porcentuales con otras. Es decir, el virus A, tiene 98,5% de similitud con el virus B.
Cuando secuenciaron los primeros casos detectados de covid-19, en Wuhan, los epidemiólogos no encontraron esa silueta, o perfil genético, en la base de datos mundial. Entendieron que era un virus nuevo. Pero al compararlo con los que existían, el análisis arrojó que era un virus similar a otros coronavirus. Era parte de la misma familia. Cuando compararon el genoma de covid-19 con otros coronavirus parecidos, salió más similar a una secuencia de coronavirus detectada en un murciélago, que a otras secuencias que afectaban humanos, como el SARS.
A medida que el SARS-CoV-2, el virus que produce covid-19, se detectó en otros países, los científicos secuenciaron más muestras y las subieron a bases de datos abiertas, se pudo entender mejor cómo el virus se movió. Cuando los virus están separados geográficamente por un tiempo suficiente, desarrollan mutaciones diferentes que eventualmente los diferencian. La cantidad de mutaciones da una idea de cuánto tiempo tiene ese virus aislado en una región geográfica.
Cada vez que un virus se replica dentro de una célula puede mutar. Una mutación es una copia del virus con una variante. La enzima que replica el ARN o ADN de los virus a veces se equivoca. Hay mutaciones que no son exitosas y por eso no las vemos; se extinguen. Hay otras que hacen al virus más exitoso o más contagioso y entonces logran transferirse a otros humanos o animales. Así evolucionan.
El zika es originario de África pero jamás había causado microcefalia al infectar mujeres embarazadas en ese continente. Al igual que otros virus, mutó. En Sudamérica, esas mutaciones diferenciaron al virus y, con el tiempo, surgió una nueva variante de la enfermedad. Cuando esa variante infecta a mujeres embarazadas, los bebés nacen con microcefalias.
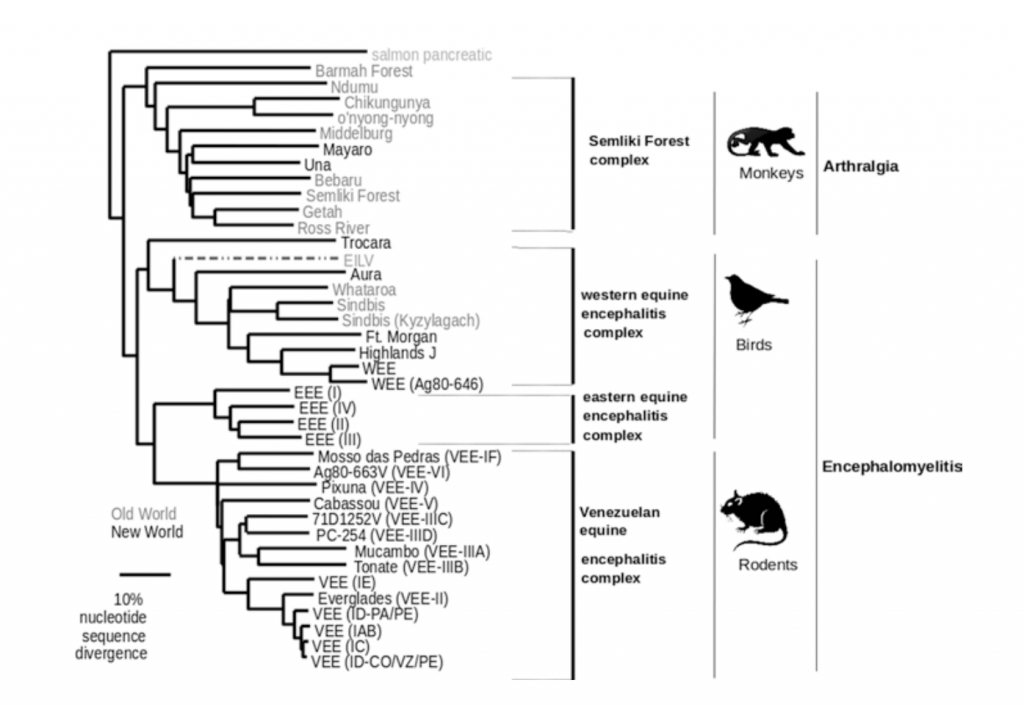
Las mutaciones ayudan a establecer árboles genealógicos del virus. Se llaman árboles filogenéticos. Los nodos representan mutaciones, puntos en los que el virus cambió. En un árbol genealógico familiar, equivaldría al nacimiento de un nuevo núcleo familiar. Algunos núcleos serán exitosos reproduciéndose y tendrán muchos hijos, que a su vez tendrán otros hijos, y estos otros, y cada generación tendrá material genético de sus ancestros.
Cada generación también tendrá una huella genética única. Pero otras familias no tendrán hijos, no podrán replicarse y su herencia genética no avanzará. Juan Carlos y otros epidemiólogos moleculares usan bases de datos mundiales que contienen millones de secuencias de virus activos hace miles años y de virus actuales, de todos los continentes, para identificar los ancestros, las familias lejanas y los parientes cercanos de cada virus. El árbol filogenético muestra la evolución del virus.
El ritmo de mutación también influye en el control de la enfermedad. Las vacunas son efectivas en la medida que el virus no cambie. Si un virus muta rápidamente, como la influenza, es menos probable que se logre una vacuna que proteja contra su infección a largo plazo. Si el virus es más estable, como la fiebre amarilla, una dosis de la vacuna puede proteger de por vida. Los virus de ARN suelen ser menos estables. Mutan más. El virus guanarito o fiebre hemorrágica venezolana, la EEV, el VIH/SIDA y el SARS-Cov-2 tiene ARN.
Después de terminar su doctorado en el centro de Galveston, Juan Carlos regresó a Venezuela al Laboratorio de Biología de Vectores del Instituto de Zoología y Ecología Tropical de la UCV. Junto con Roberto Barrera, María Eugenia Grillet y Yadira Rangel, estudiaron malaria, dengue, chikungunya, zika, EEV, Oropuche, fiebre amarilla, Mayaro, Guanarito y Encefalitis de San Luis, entre otros. Todas son zoonosis. “Venezuela tiene un clima que permite una gran diversidad de aves, mamíferos, pero también de virus. Tenemos muchos”, dice Rosa Hernández Rangel, bióloga exgerente de Diagnóstico del Departamento de Virología del INH.
Venezuela es un hotspot de zoonosis. Los hotspots se usaban en conservación para referirse a lugares con alta biodiversidad, que estaban bajo amenaza de destrucción o degradación por actividades humanas. Al mapear puntos donde surgían enfermedades, Kate E. Jones, profesora de ecología y biodiversidad en University College London, demostró que había una relación espacial directa: donde habían hotspots de alta biodiversidad, aparecían enfermedades. A partir de esta relación, Toph Allen, Peter Daszak, y otros investigadores, encontraron que las zonas más riesgosas son los bosques tropicales con cambios en el uso de la tierra, como la deforestación para la minería o la urbanización, donde hay alta biodiversidad, como Guanarito en Portuguesa.
Entre 2002 y 2019, Venezuela perdió 480.000 hectáreas de bosque húmedo tropical primario por deforestación, según Global Forest Watch. Un área equivalente a seis veces la ciudad de Nueva York. Venezuela es el catorceavo país con mayores índices de deforestación en el mundo, según la FAO (2015). Pero también es uno de los 17 países “megadiverso” del mundo, identificados en 1998 por Conservation International por tener gran biodiversidad y muchas especies endémicas.
Las zoonosis no solo ocurren cuando los humanos deforestan zonas boscosas y entran en contacto con reservorios silvestres, como los roedores en Guanarito, o cuando urbanizan zonas endémicas de vectores, como los mosquitos que transmiten malaria en el estado Bolívar. Sobre covid-19, estudios proponen que un murciélago infectó a un hospedador intermediario, algunos estudios apuntan al pangolín pero no hay consenso. Se cree que este animal fue capturado y llevado al mercado de animales silvestres vivos (wet market) de Huanan en Wuhan, China, porque los primeros casos del virus se detectaron en clientes del lugar. Pero no hay suficiente evidencia para generar consenso. No se sabe cómo saltó el virus.
A partir del 2013 el financiamiento de investigaciones epidemiológicas en Venezuela disminuyó drásticamente. El sistema de vigilancia se volvió pasivo: reaccionaba a lo que aparecía, no se adelantaba. Había personal capacitado pero no había dinero para la investigación, dice Rosa Hernández Rangel del INH. “En 2014 y 2015 hubo una ráfaga de migración de profesionales, nos fuimos quedando sin investigadores”. El laboratorio de diagnóstico de virología que detectó Guanarito tenía 13 investigadores. Cuando Rosa migró a Perú en agosto de 2019, quedaban 6.
Las instituciones con capacidad de detección se quedaron sin recursos, personal y equipos. Entre 2014 y 2018, hubo 71 robos diferentes en el Instituto de Medicina Tropical de la UCV. Extrajeron equipos especializados e infraestructura. “Es un ataque fuerte a la investigación y el gobierno no hace nada para proteger estas instituciones”, dice Rosa Hernández.
La pandemia de covid-19 llegó a Venezuela con un sistema de vigilancia epidemiológica debilitado. En el INH reclutaron a jóvenes recién graduados para hacer los diagnósticos. “Al principio se cometieron errores, se perdieron reactivos porque esos chicos no tenían la experiencia”, dice Rosa Hernández. “Han tenido que recurrir a farmacéuticos, que no tienen nada que ver con el diagnóstico de patógenos, y que no tienen experiencia con el uso de equipos o la interpretación epidemiológica”.
Diez de las once amenazas epidémicas declaradas por la Organización Mundial de la Salud en el siglo XXI son zoonosis: SARS, influenza H5N1, influenza H1N1, MERS-CoV, influenza H7N9, ébola, zika, fiebre amarilla, la peste y covid-19. Rosa cree que la capacidad para protegerse de esas enfermedades zoonóticas, radica en tener vigilancia activa: salir al campo a investigar y vigilar áreas endémicas conocidas. Juan Carlos propone retomarla mediante comités estratégicos de expertos en zoonosis. “Deberíamos tener un centro tipo CDC de Estados Unidos, de investigación y control, que funcione en conjunto con el ministerio de salud, las universidades y los centros de investigación”.
Juan Carlos emigró a Quito en 2014 para asesorar al Centro Internacional de Zoonosis de la Universidad Central de Ecuador. Desde 2016 dirige el programa de investigación de la Facultad de Ciencias Naturales y Ambientales de la Universidad Internacional SEK e investiga enfermedades emergentes en la amazonía ecuatoriana. En marzo usó la evolución de casos del virus en tiempo real para dictar clases de virología, y deconstruyó noticias falsas sobre el virus para explicar su epidemiología molecular. “Son tiempos importantes para lo que hacemos”.
***Esta es una historia de Helena Carpio en el marco del proyecto de Prodavinci y el Centro Pulitzer: COVID-19 llega a un país en crisis: Despachos desde Venezuela.












































